腸道屏障修復完全指南:腸漏症、SIBO 與 4R 營養治療策略
你的腸道「城牆」還穩固嗎?——專科營養師 Jim Lau 的系統修復方案
作者:Jim Lau(劉嘉豪)|腸胃科註冊營養師
澳洲坎培拉大學營養治療碩士 · 香港中文大學食品及營養科學一級榮譽畢業 · TECH Global University 腸道微生態研究生文憑
Nutrition Point 營養治療中心創辦人|尖沙咀麼地道 62 號永安廣場 1 樓 128 號
發佈日期:2026 年 2 月 28 日
腸道屏障是人體與外界環境之間最重要的一道防線。這條長達六至七米的消化管道,每天承受數以萬計的食物抗原、細菌代謝物及潛在有害物質的衝擊。當腸道屏障完整而堅固時,營養素被精準吸收、毒素被有效阻隔;但一旦屏障功能崩塌——也就是坊間常說的「腸漏症」(Leaky Gut)——後果遠不止腹脹、腹瀉那麼簡單。從濕疹反覆發作到慢性疲勞、自體免疫疾病,大量臨床研究已證實這些看似不相關的症狀,往往都源於同一個起點:受損的腸道屏障。作為專注腸道營養治療的臨床營養師,我將在本文為你系統拆解腸道屏障的運作機制、腸漏症與 SIBO 的深層成因,以及經臨床驗證的 4R 修復原則,為你提供一套從根源修復腸道健康的完整方案。
腸道屏障——人體最重要的「城牆」如何運作?
要修復腸道屏障,首先要理解它的運作原理。腸道屏障並非一層簡單的細胞膜,而是由三重精密防線協同構成的立體防禦系統。
第一道防線:腸道菌群(Gut Microbiota)
腸道內棲息着超過 100 兆微生物,構成一個龐大的「生態守衛軍」。這些有益菌透過多重機制保護屏障:它們佔據腸壁表面阻止致病菌定殖,更會產生短鏈脂肪酸(Short-Chain Fatty Acids, SCFAs),當中最關鍵的丁酸(Butyrate)是腸道上皮細胞的首選能量來源,直接滋養腸壁細胞、促進屏障修復。菌群失衡(Dysbiosis)會導致丁酸產量下降,腸壁細胞「斷糧」,屏障強度隨之減弱。
第二道防線:黏液層(Mucus Layer)
腸壁表面覆蓋着由杯狀細胞(Goblet Cells)分泌的黏蛋白(Mucin)所形成的保護性黏液層。這層黏液如同城牆外的護城河,物理性地隔離腸腔內容物與上皮細胞。黏液層分為內外兩層:外層較為疏鬆,容許共生菌棲息;內層則極為緻密,形成幾乎無菌的保護帶。當飲食缺乏膳食纖維時,腸道菌群可能轉而「啃食」黏液層作為能量來源,令這道天然屏障日漸薄弱。
第三道防線:緊密連接(Tight Junctions)
腸道上皮細胞之間由精密的蛋白質複合體緊密連接在一起,這是屏障最核心的結構基礎。主要的緊密連接蛋白包括:
- -Claudin 蛋白家族——構成緊密連接的骨幹結構,決定細胞間隙的通透性選擇
- -Occludin——穩定緊密連接的完整性,調節細胞旁路運輸
- –ZO-1(Zonula Occludens-1)——連接緊密連接蛋白與細胞骨架的橋樑蛋白
- -Zonulin——唯一已知能可逆性調節緊密連接開關的生理性蛋白
Zonulin 是理解腸漏症的關鍵分子。當 Zonulin 過度釋放時,它會降低 ZO-1 表達,使緊密連接「鬆開」,腸道通透性隨之增加。Nature Communications(2020)的研究明確指出 Zonulin 是觸發關節炎的分子因素,其機制正是透過調控腸道屏障功能、減少 ZO-1 表達、增加腸道通透性,讓腸腔內的抗原進入血液循環引發全身性免疫反應。
臨床生物標記最新進展:2025 年發表於Frontiers in Medicine 的研究發現,血清 Claudin-3(AUC=0.934)和 Zonulin(AUC=0.826)是評估腸道屏障功能障礙的重要生物標記。其中 Claudin-3 更能直接反映結構性損傷,而 Zonulin 則反映緊密連接的功能性調節狀態。兩者配合使用,可更全面評估屏障完整性。
腸漏症(Leaky Gut)全面剖析——成因、症狀與全身發炎的連鎖反應
當上述三重防線受損,腸道屏障的通透性異常增加,未完全消化的食物分子、細菌毒素和其他抗原便會穿越屏障進入血液循環——這就是「腸漏症」的核心病理。
腸漏症的常見成因
- –食物敏感——麩質(Gluten)是已知最強的 Zonulin 釋放觸發因子,即使在非乳糜瀉患者中也可增加腸道通透性
- –慢性壓力——皮質醇持續升高會直接破壞緊密連接蛋白、抑制腸壁修復
- –藥物影響——質子泵抑制劑(PPI)長期使用會改變腸道酸鹼環境及菌群組成;非類固醇消炎藥(NSAIDs)直接損傷腸黏膜
- –酒精——乙醇及其代謝物乙醛會破壞緊密連接蛋白的磷酸化狀態
- –高糖高脂飲食——促進促炎菌群增生,減少產丁酸菌比例
- –飲食因素中的紅肉與甜味穀物——2025 年針對電競選手的研究發現 85.74% 受試者的 Zonulin 水平偏高,且紅肉和甜味穀物攝取量與 Zonulin 呈正相關;BMI 與 Zonulin 之間亦存在顯著正相關(R=0.49, p<0.001)
從腸漏到全身發炎的連鎖反應
腸漏症的影響遠超消化系統本身。當腸道屏障破損,革蘭氏陰性菌的細胞壁成分——脂多醣(LPS, Lipopolysaccharide)會大量進入血液循環,這一過程稱為「代謝性內毒素血症」。LPS 與免疫細胞表面的 TLR4 受體結合後,啟動 NF-κB 信號通路,引發全身性促炎細胞因子風暴(TNF-α、IL-6、IL-1β),最終導致一系列慢性發炎相關疾病:
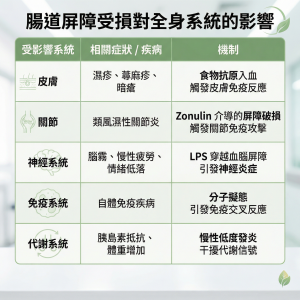
Nature Molecular Psychiatry 的薈萃分析進一步確認,嚴重精神疾病及慢性疲勞綜合症患者體內的 Zonulin、LPS 和 LBP(LPS 結合蛋白)均顯著高於對照組,而腸道菌群失衡的生物標記與疾病行為嚴重程度呈正相關。這有力地證明了腸道屏障受損與全身性疾病之間的因果鏈條。
更值得關注的是,Nature Communications(2020)的研究發現,使用 Zonulin 拮抗劑 Larazotide Acetate 能恢復屏障功能並減輕關節炎症狀,這從治療層面反向驗證了腸漏在自體免疫疾病中的關鍵角色。
SIBO(小腸細菌過度增生)深度解析
SIBO(Small Intestinal Bacterial Overgrowth, 小腸細菌過度增生)是腸道屏障問題的另一個重要環節。正常情況下,小腸內的細菌數量相對稀少,大部分腸道菌群集中在大腸。當小腸內的細菌異常增殖,它們會過度發酵食物殘渣(尤其是碳水化合物),產生大量氣體並損傷腸黏膜,加劇屏障破損。
SIBO 的成因與類型
SIBO 的發生與多種因素相關:移行性複合運動(MMC, Migrating Motor Complex)功能低下使小腸的「清掃」能力減弱;胃酸不足(常見於長期使用 PPI 的患者)令細菌在上消化道存活繁殖;迴盲瓣功能不全導致大腸菌群逆流入小腸。此外,幽門螺旋桿菌(H. pylori)感染亦與 SIBO 風險增加有關聯。
根據產生的氣體類型,SIBO 可分為三種亞型:
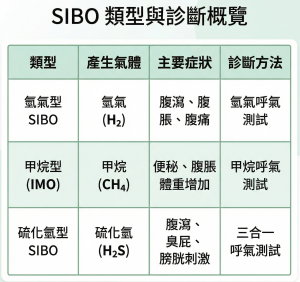
為什麼「多吃蔬果」反而可能加劇 SIBO?
這是很多患者甚至部分醫療專業人士的常見盲點。蔬菜和水果含有大量可發酵碳水化合物(Fermentable Carbohydrates),包括果聚糖、半乳聚糖、乳糖、果糖和多元醇——也就是 FODMAP(Fermentable Oligosaccharides, Disaccharides, Monosaccharides And Polyols)。在 SIBO 患者的小腸中,這些物質恰恰是過度增殖細菌的「糧食」,攝取越多,細菌發酵越旺盛,產氣越嚴重,症狀越惡化。因此,善意的「多吃蔬果」建議,在 SIBO 患者身上可能適得其反。
低 FODMAP 飲食的三階段策略
低 FODMAP 飲食是目前治療 SIBO 及 IBS 最具循證基礎的飲食策略之一。根據美國胃腸病學院(ACG)的指引,低 FODMAP 飲食包含三個階段:
- 限制期(Elimination Phase, 2-4 週)——嚴格限制所有高 FODMAP 食物,讓腸道症狀穩定下來
- 重新引入期(Reintroduction Phase)——逐一重新引入各類 FODMAP,識別個人觸發食物
- 個人化維持期(Personalization Phase)——根據個人耐受程度制定長期飲食方案
Nutrients(2025)的綜述指出,SIBO 在治療後九個月內的復發率高達 43%,因此營養與飲食治療在長期管理中扮演至關重要的角色。該研究還強調,餐與餐之間保持約 5 小時間隔有助支持 MMC 的正常「清掃」功能,減少 SIBO 復發風險。此外,Practical Gastroenterology(2025)提出了「FODMAP Gentle」和「FODMAP Simple」等新興溫和版策略,讓對嚴格限制飲食感到困難的患者也能獲益,但強調由註冊營養師主導實施至關重要。
4R 腸道修復原則——營養師的系統治療框架
4R 原則(Remove, Repair, Replace, Reinoculate)是功能醫學營養師修復腸道屏障最系統化的治療框架。每一個 R 環環相扣,缺一不可。
第一步:Remove(移除)——清除致敏源與病原
治療的第一步是找出並移除損害腸道屏障的因素。這包括:透過排除飲食法(Elimination Diet)識別並移除致敏食物,最常見的觸發因子包括麩質、乳製品(尤其 A1 酪蛋白)、精製糖和高度加工食品;同時處理潛在感染,包括 SIBO、念珠菌過度增生(Candida Overgrowth)和寄生蟲感染;減少環境毒素暴露。這一步是整個 4R 方案的基礎——如果致敏因子未被移除,後續修復無從談起。
第二步:Repair(修復)——修補受損黏膜
在移除致敏源後,下一步是為腸壁提供修復所需的關鍵營養素:
- L-Glutamine(L-谷氨酰胺)——腸上皮細胞的首選燃料,建議劑量每日 >5g。發表於 Gut 期刊的隨機對照試驗(約 100 名 IBS 患者)顯示,口服 L-Glutamine 能顯著正常化腸道通透性指標(LMR, Lactulose-Mannitol Ratio)
- 鋅(Zinc, 每日 8-11mg)——維持緊密連接蛋白的結構完整性,缺鋅會直接導致緊密連接鬆弛
- Omega-3 脂肪酸(EPA/DHA)——抑制 NF-κB 信號通路、減少腸道促炎細胞因子釋放
- 維他命 D——上調有益菌群比例、促進抗菌肽分泌、支持腸壁細胞修復與分化
第三步:Replace(補充)——優化消化能力
許多腸道屏障受損的患者同時存在消化功能低下的問題,食物未能被充分消化便進入腸道,加重菌群發酵和屏障壓力。需要補充的包括:
- 消化酶(Digestive Enzymes)——蛋白酶、脂肪酶、澱粉酶,幫助食物在上消化道充分分解
- 鹽酸甜菜鹼(HCl / Betaine HCl)——針對胃酸不足的患者,恢復胃部的正常酸度和消毒功能
- 膽鹽(Bile Salts)——輔助脂肪消化吸收,對膽囊功能低下或膽囊切除患者尤為重要
第四步:Reinoculate(接種)——針對性補充益生菌
修復腸道菌群生態是鞏固屏障的最後一步。重點不在於「多吃益生菌」,而在於精準選擇菌株:
- Lactobacillus 和 Bifidobacterium 菌屬——多項研究證實其能增強緊密連接蛋白表達、促進黏液分泌
- 布拉氏酵母菌(Saccharomyces boulardii)——這是 4R 方案中特別值得關注的菌株
S. boulardii 的獨特優勢在於它是酵母菌而非細菌,因此不受同時使用的抗生素影響。Nutrients(2025)的綜述指出,S. boulardii 與抗生素聯合使用可達到最高的 SIBO 根除率。Drugs in Real World Outcomes(2024)的研究更顯示,S. boulardii CNCM I-745 在腹瀉治療中達到 77.8% 的止瀉率,對照組僅 15.8%(OR=18.7)。此外,Pediatric Research(2025)的研究證實 S. boulardii 能顯著改善兒童 IBS-D 症狀並減輕炎症反應。
4R 原則要點速覽:移除致敏源 → 修復腸黏膜 → 優化消化能力 → 精準補充益生菌。四步驟環環相扣,由營養師根據個人體質度身制定方案,才能達致最佳修復效果。
食物敏感性濕疹——腸道屏障受損的皮膚警號
濕疹是腸道屏障受損最直觀的「皮膚警報器」。愈來愈多研究揭示了「腸—皮軸」(Gut-Skin Axis)的存在:腸道微生態失衡 → 腸漏 → 食物抗原入血 → 皮膚炎症,這條完整的病理鏈條解釋了為何單純塗抹外用藥膏往往只能暫時壓制症狀。
International Journal of Molecular Medicine(2025)的腸—皮軸綜述指出,當腸道屏障破損,微生物代謝物和食物抗原進入全身循環,透過 T 細胞分化和細胞因子表達影響皮膚屏障功能;而腸道菌群產生的短鏈脂肪酸能抑制促炎細胞因子,從內部維護皮膚健康。Pediatric Allergy and Immunology(2025)的研究進一步發現,濕疹患者的腸道菌群多樣性(尤其是雙歧桿菌)顯著降低,腸道通透性增加讓食物抗原得以通過腸—皮軸觸發皮膚炎症。Long 等人的孟德爾隨機化研究更從因果層面確立了腸道菌群與濕疹、暗瘡、銀屑病、玫瑰痤瘡之間的因果關係。
I-A 型濕疹體質:「濕 = 未消化的食物」
在 Nutrition Point 的臨床體質分類中,I-A 型濕疹體質的核心概念是「濕 = 未消化的食物」。這類患者因基因體質上無法有效儲存維他命 B12 和葉酸,導致胃酸分泌不足。當動物蛋白質和脂肪未能被充分消化時,含硫毒素和「濕氣」進入血液循環,最終以濕疹形式在皮膚表現出來。
- –關鍵缺乏營養素:B12、硒(Selenium)
- –典型症狀:腹脹、多氣、睡眠質素差、濕疹反覆發作但找不到明確食物誘因
- –飲食策略:以植物性蛋白為主(魚類、豆類),選擇易消化的穀物(白藜麥、白米、米粉),搭配綠色水果,蔬菜量控制在半碗以下且選擇質地柔軟的品種,避免牛奶改用其他奶類
I-B 型濕疹體質:消化酶缺乏的急性反應
I-B 型體質同樣遵循「濕 = 未消化食物」的核心原則,但機制有所不同。這類患者因無法有效儲存維他命 B6、B2 或 B1,導致消化酶(尤其是分解蛋白質和脂肪的酶)產生不足。紅肉中的蛋白質和脂肪未被充分分解,脂肪毒素在腸道內發酵產生「濕氣」,進入循環系統後引發急性濕疹。
- –關鍵缺乏營養素:B6、鈣,可能伴隨 B2 缺乏
- –典型症狀:便秘、消化不良、急性濕疹發作、對紅肉和小麥製品反應強烈
- –飲食策略:間歇性低碳水飲食,以白肉和海鮮為主要蛋白質來源,嚴格避免紅肉和小麥製品

Jim Lau 營養師的臨床 4R 實踐
理論框架再完善,最終仍需落地為可執行的管理方案。在 Nutrition Point 的臨床實踐中,
我們採用「雙軌互補系統」(Dual-Track Complementary System),結合兩項功能評估工
具,將 4R 原則精準落實到每位個案身上。
微元素狀態評估——讀取身體的「營養藍圖」
微元素狀態評估以生物電阻抗分析(BIA)技術為基礎,透過皮膚生物電阻抗評估 18 種
以上營養素的儲存水平。由於皮膚細胞的更新週期約為 28 天,評估結果反映的是長期營
養儲備而非即時波動,因此能揭示個人的體質傾向——即身體天生的營養代謝特性。透
過微元素評估,營養師可以確定個案屬於 A1、B1、B2、I-A 或 I-B 等不同體質類型,作
為制定營養管理方案的根本依據。
健康狀態 NLS 指標分析——啟動 24 小時健康預警系統
NLS(Non-Linear System)指標分析是基於能量熵原理的非入侵性評估方式,可涵蓋 215
個以上器官和組織的生理狀態掃描。系統透過嚴重程度標記顯示不同級別的失衡信號:
黃色——理想狀態
紅色三角——中度壓力/失衡
黑色方塊——高度壓力/失衡
狀態頻譜標記則進一步細分:△ 代表低度壓力或能量不足,▽ 代表生理性反應,◇ 代表
失衡初起,□ 代表信號干擾。NLS 的更新週期為 7 天,專有的健康指數評分系統以 0-2
為低風險、3-5 為中度風險、6 分以上為高風險。
雙軌互補的臨床流程
我們的核心理念是:「先用 NLS 找熱點,再用微元素讀藍圖。」微元素評估猶如營養藍
圖(Nutritional Blueprint),揭示體質的根本結構;NLS 則是 24 小時預警系統(Early
Warning System),即時偵測當下的生理壓力熱點。藍圖加上預警系統,才能實現真正的
精準營養管理。
臨床五步流程:
- –步驟一:微元素狀態評估 → 建立個人體質藍圖(A1、B1、B2、I-A、I-B)
- –步驟二:NLS 指標分析 → 掃描當前生理壓力熱點
- –步驟三:交叉比對藍圖 + 警報 → 制定個人化營養方案
- –步驟四:定期 NLS 跟進(7-45天) → 短期進度追蹤
- –步驟五:定期微元素跟進(1-3 個月) → 長期改善驗證
臨床邏輯示例
同樣是 NLS 顯示腸道壓力信號,對不同體質的處理方式截然不同。以 A1 型體質為例,
營養師會優先考慮是否使用了不適合的蛋白質來源(如過量紅肉)導致消化負擔過重;而對於 I-B 型體質,則會考慮小麥或紅肉是否觸發了消化效率下降的連鎖反應。這種「同一
警報、不同解讀」的思維模式,正是精準營養管理與一刀切飲食建議的根本分別。
基於體質分型和健康指標的結果,我們會為每位個案制定個人化的食療方案和營養補充搭
配:選擇適合體質的蛋白質來源、穀物類型、蔬果比例,同時精準補充該體質所缺乏的微
量營養素,使 4R 修復方案真正做到「因人而異」。
(註:NLS 指標分析和微元素狀態評估均為功能性營養評估工具,並非醫學診斷儀器。所
有結果必須由合資格營養師結合專業判斷進行綜合解讀,不取代任何醫學建議或診斷。)
常見問題(FAQ)
Q1:腸漏現象可以通過普通血液檢測確診嗎?
–目前臨床上主要透過生物標記評估腸道屏障狀態。血清 Zonulin 反映緊密連接的功能調節
狀態;Claudin-3 則能反映腸壁結構性狀態——2025 年 Frontiers in Medicine 的研究顯示
Claudin-3 的指標具有優異的參考價值。傳統的乳果糖-甘露醇比率測試(LMR)可評估腸
道通透性,但操作較繁瑣。在我們的臨床實踐中,NLS 指標分析作為功能性評估的輔助
方案,能非入侵性地評估腸道及全身生理壓力狀態,為營養決策提供即時參考,但需注意
其為功能性評估工具而非醫學診斷。
Q2:SIBO 人士可以食益生菌嗎?
–視乎情況而定。部分細菌性益生菌可能在 SIBO 活躍期加重氣體產生,因為它們本身也
可能在小腸中發酵。相比之下,布拉氏酵母菌(Saccharomyces boulardii)是 SIBO 人士
的常用選擇——它屬於酵母菌而非細菌,不受同時使用的抗生素影響。Nutrients(2025)
的綜述指出 S. boulardii 在管理中展現良好潛力。但具體的益生菌選擇仍需根據 SIBO 亞
型和個人狀況由營養師個別評估。
Q3:4R 修復需要多長時間才能見效?
–因人而異。一些人士在開始 4R 方案後數週內便能感受到腹脹減輕、精力改善等初步變
化;但腸道屏障的完整修復通常需要 3 至 6 個月。影響進度的因素包括屏障受損程度、
體質類型、飲食依從性和壓力管理。在我們的臨床流程中,透過 NLS 指標分析(每 7-14
天跟進)可追蹤短期進度變化,而微元素狀態評估(每 1-3 個月跟進)則驗證長期營養改
善狀況,確保方向正確。
Q4:食物敏感和食物過敏有什麼分別?
–兩者機制完全不同。食物過敏(Food Allergy)由 IgE 抗體介導,反應在數分鐘至數小時
內出現,屬於即時型免疫反應。食物敏感(Food Sensitivity)則通常由 IgG 或 IgA 抗體介
導,反應往往延遲數小時至數天,表現為慢性低度反應,如腹脹、疲勞、皮膚不適、頭痛
等。關鍵在於:腸道屏障狀態會影響食物敏感的風險——當屏障功能下降,原本不應進入
血液的食物大分子得以穿越屏障,可能觸發免疫系統對更多食物產生反應。










